一、钠
1、钠的物理性质 钠是一种质软、银白色、有金属光泽的金属,具有良好的导电性、导热性,密度比水小,比煤油大,熔点较低。 2、钠的化学性质 (1)与非金属反应: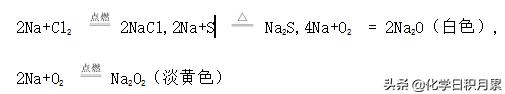
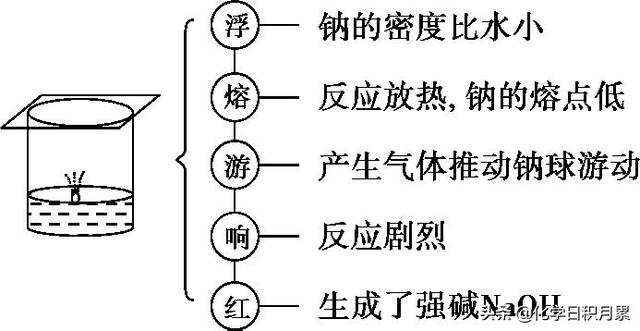
- 钠投入到饱和NaCl溶液中,有H2产生,同时有NaCl晶体析出(恢复至原温度)。
- 钠投入到NH4Cl溶液中,有H2和NH3逸出。
- 钠投入到CuSO4溶液中,有H2产生并有蓝色沉淀Cu(OH)2生成。

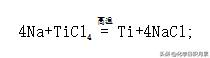
二、钠的重要化合物
1、钠的氧化物的比较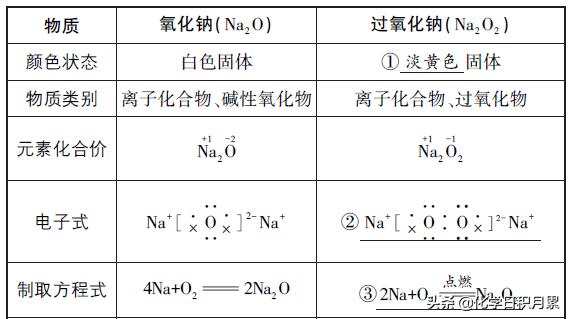
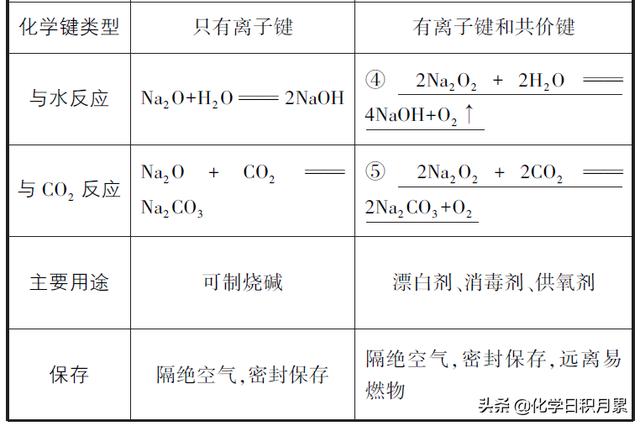
- 1)颜色状态:白色固体。
- 2)俗称:烧碱、火碱、苛性钠。
- 3)溶解性:易溶于水。
- 4)潮解:在空气中容易潮解,在实验室中可用固体NaOH作干燥剂。
- 1)NaOH溶于水后完全电离,能使酸碱指示剂变色。
- 2)与酸和酚发生反应,如HCl、CH3COOH、C6H5OH等。
- 3)与酸酐发生反应,如SO2、CO2、SiO2、SO3、P2O5和(CH3CO)2O等。
- 4)与某些非金属单质反应,如Cl2、S等。
- 5)与两性氧化物、两性氢氧化物反应,如Al2O3、Al(OH)3等。
- 6)与盐发生复分解反应,如含NH4 、Cu2 、HCO3-、H2PO4-、HSO3-等的盐。
- 7)提供碱性环境发生有机反应,如卤代烃的水解反应和消去反应、油脂的皂化反应等。
- 原理(电解饱和食盐水):
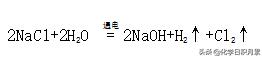
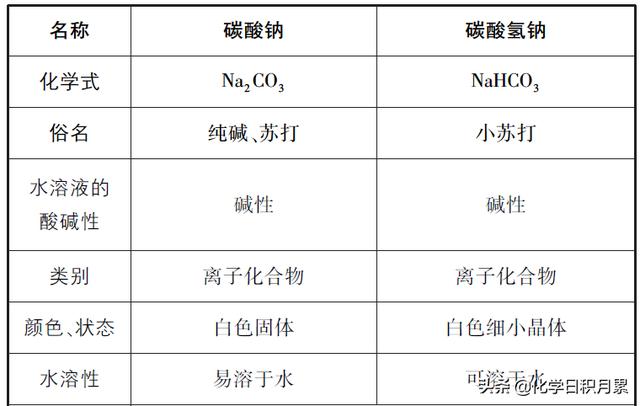
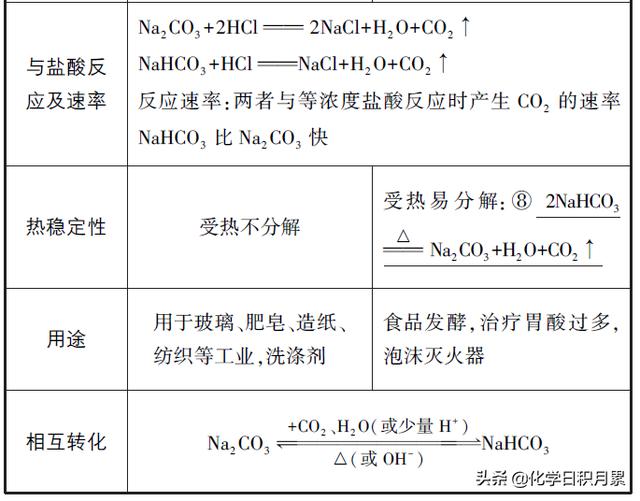
- a.点燃酒精灯。
- b.将铂丝放入稀盐酸中清洗,再放到酒精灯外焰上灼烧,直至火焰呈现原来的颜色。
- c.用铂丝蘸取待测物,在酒精灯外焰上灼烧,观察火焰的颜色[在观察钾元素的火焰颜色时,应透过蓝色钴玻璃(可滤去掩盖紫色的黄光)]。
- d.将铂丝用稀盐酸洗净后,在酒精灯外焰上灼烧至没有颜色,再做其他实验。



本站内容收集整理于网络,多标有原文出处,本站仅提供信息存储空间服务。如若转载,请注明出处。