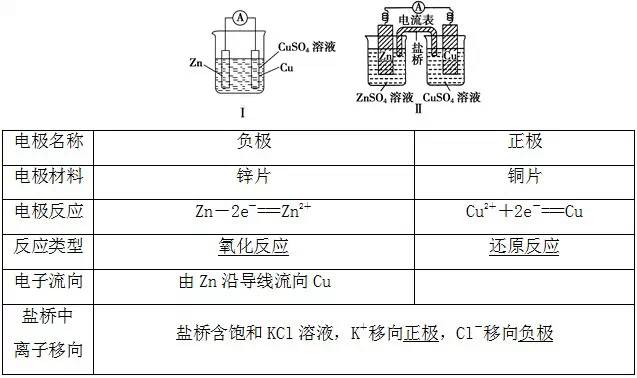
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)。(3)三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接触;③两电极插入电解质溶液。
考点2:电解池
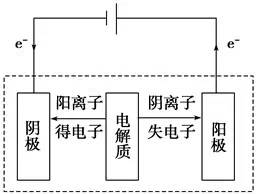
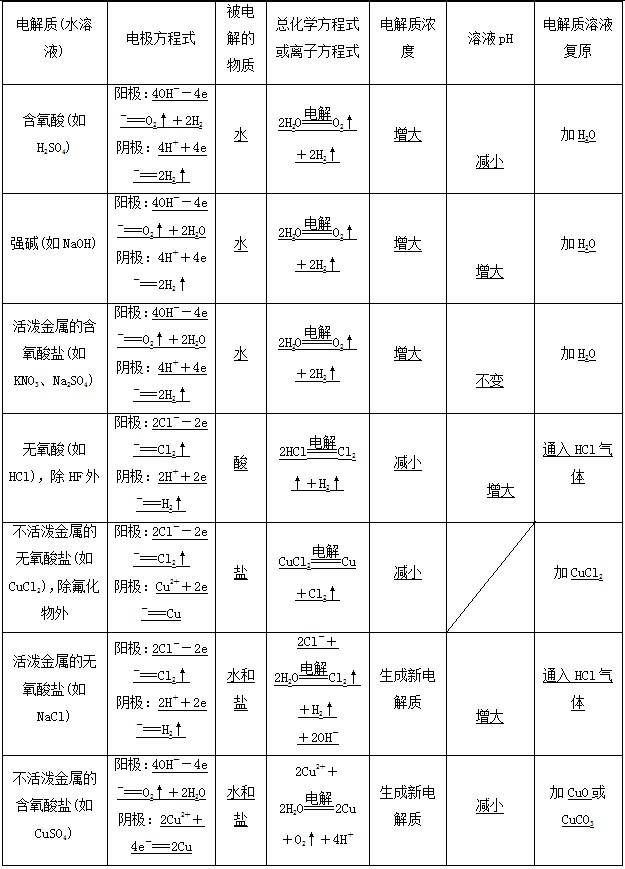
在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。首先看电极,如果阳极是活性电极(金属活动顺序表Ag以前的金属),则阳极电极材料失电子,电极溶解,溶液中的阴离子不能失电子。如果是惰性电极(Pt、Au、石墨),则再看溶液中的阴离子的失电子能力。此时阴离子放电顺序:活泼电极>S2->I->Br->Cl->OH->含氧酸根离子。阳离子放电顺序:Ag >Fe3 >Cu2 >H (酸)>Fe2 >Zn2 >H (水)>Al3 >Mg2 >Na >Ca2 >K 。阳极反应式:2Cl--2e-===Cl2↑(氧化反应)下图为金属表面镀银的工作示意图,据此回答下列问题:(2)电解质溶液是AgNO3溶液等含镀层金属阳离子的盐溶液。(4)特点:阳极溶解,阴极沉积,电镀液的浓度不变。利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。阳极:6O2--12e-===3O2↑;阴极:4Al3 12e-===4Al。
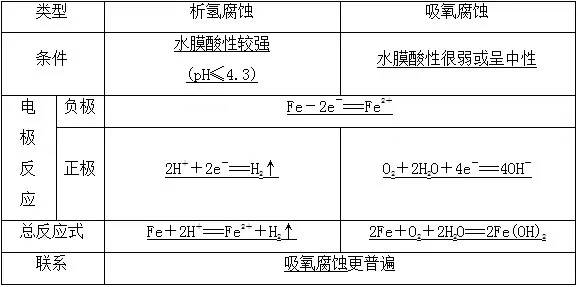
考点3:金属的腐蚀和保护
金属原子失去电子变为金属阳离子,金属发生氧化反应。(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。 本站内容收集整理于网络,多标有原文出处,本站仅提供信息存储空间服务。如若转载,请注明出处。